Версия для слабовидящих
- 1. ОСНОВЫ МАТЕРИАЛОВЕДЕНИЯ
- 2. ОСНОВЫ ЭЛЕКТРОТЕХНИКИ
- 3. НОРМАТИВНО-ТЕХНИЧЕСКАЯ ДОКУМЕНТАЦИЯ
- 4. ЧТЕНИЕ СХЕМ И ЧЕРТЕЖЕЙ
- 5. ОСНОВЫ ОБЩЕЙ ХИМИИ
- 6. ТРЕБОВАНИЯ ПРОМЫШЛЕННОЙ БЕЗОПАСНОСТИ И ОХРАНЫ ТРУДА
- 7. НЕФТЬ И ЕЕ СВОЙСТВА. ХРАНЕНИЕ И ТРАНСПОРТИРОВКА НЕФТИ И НЕФТЕПРОДУКТОВ
- 8. ЭКСПЛУАТАЦИЯ ТЕХНОЛОГИЧЕСКОГО ОБОРУДОВАНИЯ, РЕЗЕРВУАРОВ И ТРУБОПРОВОДОВ
- 9. ПРАВИЛА ТЕХНИЧЕСКОЙ ЭКСПЛУАТАЦИИ НЕФТЕБАЗ
- ИТОГОВЫЙ МЕЖДИСЦИПЛИНАРНЫЙ ЭКЗАМЕН
1.1. Основы материаловедения
Почти до конца XVIII в. принято было считать, что существует только семь металлов: золото, серебро, ртуть, медь, железо, олово и свинец. Золото и серебро, которые не изменяются под действием воздуха, влаги и высокой температуры, получили название драгоценные металлы. Остальные металлы, которые под действием воды и воздуха теряют металлический блеск, покрываются налетом, а после прокаливания превращаются в рыхлые окалины, назвали недрагоценные. Такое деление металлов применяют и сейчас, но с тем отличием, что к двум уже названным металлам добавили открытые позднее платину и пять ее спутников: палладий, родий, иридий, осмий и рутений. Эти восемь перечисленных элементов и составляют группу драгоценных металлов.
В России документами, которые регламентируют все связанное с драгоценными металлами (термины, марки сплавов, методы испытания свойств определение химического состава и пробы, способы переработки отходов и др.) являются государственные стандарты.
Так, согласно государственному стандарту драгоценный металл (Precious metal) – это цветной металл, обладающий высокой химической стойкостью в агрессивных средах, тугоплавкостью, ковкостью, тягучестью. К драгоценным металлам относятся золото, серебро, платина и металлы платиновой группы – палладий, иридий, родий, рутений и осмий. Этот перечень может быть изменен только федеральным законом Российской Федерации. Драгоценный металл может находиться в самородном и аффинированном видах, в сырье, сплавах, продуктах металлургического производства, химических соединениях, ювелирных и иных изделиях, отходах производства и потребления. Для драгоценных металлов часто используют термин благородный металл, хотя этот термин не рекомендован для применения указанным выше государственным стандартом. Благородным металлом принято считать металл, у которого, во- первых, электродный потенциал является высоко положительным относительно водородного электрода, а во-вторых, такой металл должен быть особенно стойким к окислению и обладать выраженным противодействием химической реакции в растворах неорганических кислот. Основные термины, относящиеся к драгоценным металлам, сформулированы в ГОСТ Р 52793-2007 Металлы драгоценные. Термины и определения. Далее приведем выдержки из этого документа.
Металл платиновой группы – это драгоценный металл, сопутствующий платине в рудах и имеющий схожие свойства с ней и с другими металлами этой группы. К платиновой группе относят палладий и редкие металлы платиновой группы иридий, родий, рутений и осмий.
Драгоценные металлы отличаются от других металлов физическими, химическими свойствами и стоимостью, что определяет их особое положение среди остальных металлических материалов.
Исключительно высокие антикоррозионные свойства в различных агрессивных средах и декоративный вид делают драгоценные металлы незаменимыми в быту в качестве ювелирных изделий, орденов, медалей, значков, гигиенической высокохудожественной посуды, столовых приборов и т.п., а также в технике, где они находят все большее применение благодаря другим своим показателям. Например, из них изготовляют различные контакты и ответственные токопроводы, постоянные магниты (Pt – Co), катализаторы, фильеры для стекловолокна, лабораторную посуду, медицинские принадлежности, аппаратуру для электролиза, термопары, шкалы приборов, эталоны и другие изделия. Драгоценные металлы широко применяются для создания антикоррозионных покрытий ответственных деталей приборов, всевозможных зеркальных отражателей, эффективных электрохимических источников тока и подшипников скольжения, медицинских препаратов, бактерицидных фильтров, кино-, фото- и рентгенопленок, фотобумаги, токопроводящих клеев, нерастворимых анодов, ответственной пайки изделий и других целей. Ранее большие объемы драгоценных металлов, особенно серебро, применяли для производства разменной монеты. Однако острый недостаток серебра для использования в промышленных целях вынудил заменить этот металл в разменной монете другими, менее дефицитными металлами (никелем, алюминием, магнием и т.д. в сплавах с другими металлами).
Особенно широко применяются в быту и технике драгоценные металлы в сплавах между собой и с другими металлами. Легирование драгоценных металлов различными компонентами позволяет существенно изменять и варьировать в огромном диапазоне их физико-химические и другие свойства в соответствии с назначением и потребностями, а также обеспечивать эффективную экономию и снижение стоимости изготовляемых изделий.
Постоянное развитие техники, а также повышение требований потребителя к качеству ювелирных изделий требуют усовершенствования нормализации и стандартизации производства драгоценных металлов, их обработки и потребления. В результате были пересмотрены государственные стандарты на марки драгоценных металлов в слитках и порошках, полуфабрикатах и изделиях. Изменениям подверглись также стандарты на методы анализа драгоценных металлов. Перечисленные стандарты постоянно перерабатываются с учетом совершенствования методов производства драгоценных металлов и изделий из них.
Непрерывное повышение спроса промышленности и населения на изделия, полученные из драгоценных металлов, или покрытые такими металлами, а также рост потребности ряда отраслей в чистых драгоценных металлах для специальных целей поставило задачу по нахождению новых источников добычи и методов максимального извлечения драгоценных металлов из руд. К таким источникам можно также отнести разработку новых эффективных технологий улучшения сбора и методов переработки и аффинажа вторичного сырья в виде лома, отходов, солей и растворов, содержащих драгоценные металлы.
Классификация драгоценных металлов и сплавов, по сравнению с классификациями других металлов и сплавов, имеет ряд принципиальных отличий, к которым можно отнести:
- обособленность и самостоятельность всей этой группы металлов и содержащих их сплавов относительно других групп металлов и сплавов;
- особый порядок построения марок сплавов, содержащих драгоценные металлы, особое обозначение марок этих сплавов и особое общее и частное наименование сплавов в случаях, когда драгоценные металлы не являются в них основными компонентами или когда в сплавах для изготовления изделий бытового назначения присутствует в качестве компонента наряду с другими драгоценными металлами золото;
- особое исчисление и особое количественное выражение числовых значений содержания золота, серебра, платины и палладия в марках драгоценных металлов и сплавов в полуфабрикатах и изготовляемых из них изделий, поступающих в обращение к населению или имеющих музейно- выставочное и другое специальное назначение.
Отличия эти сложились исторически на основе многовековой мировой практики производства, апробирования, учета, нормирования, продажи, купли и потребления этих металлов и сплавов, а также издавна и почти повсеместно осуществляемого специального пробирного надзора и поэтому стали узаконенными постановлениями правительств многих стран и международных соответствующих организаций, а также всеобщей традицией.
Причина же возникновения и сохранения в том же виде этих традиций – особая роль драгоценных металлов, которую они играют в валютно- финансовых, банковских, таможенных и других сферах, не свойственная другим металлам; исключительное положение в сфере бытового и специального потребления; особая значимость в технике и осуществлении дальнейшего технического прогресса, где они находят все большее применение и во многих случаях незаменимы другими металлами, а также их высокая стоимость и крайняя ограниченность распространения и добычи.
Физико-химические и механические свойства драгоценных металлов и сплавов, определяющие их поведение при технологических процессах и эксплуатации, зависят от атомного строения, характеризуемого периодической системой элементов Д.И.Менделеева. Все драгоценные металлы относятся к переходным металлам. Серебро и золото входят наряду с медью в группу ІБ; рутений, родий, палладий, осмий, иридий, и платина – в группу VІІІБ наряду с железом, кобальтом и никелем. Для всех перечисленных металлов характерна высокая прочность межатомной связи, которая определяет кристаллическую структуру и физические свойства металлов и сплавов.
Драгоценные металлы обладают кристаллической структурой с наиболее плотной атомной упаковкой (координационное число 12) гексагональной плотноупакованной (г.п.у.) и гранецентрированной кубической (г.ц.к.). Первый тип решетки имеют рутений и осмий, а остальные - г.ц.к. решетку.
Физические свойства
Плотность. Драгоценные металлы по плотности следует разделить на две группы: легкие и тяжелые. Плотность серебра, рутения, палладия и родия значительно ниже плотности золота и их относят к легким драгоценным металлам. Золото, платину, иридий и осмий называют тяжелыми драгоценными металлами, из которых два последних – наиболее плотные вещества.
Температура плавления. В настоящее время температура и теплота плавления золота, серебра и платины определены для содержания в них примесей менее 0,01%. Для родия, иридия и рутения эти данные определены для содержания примесей 0,03, 0,05 и 0,02%, соответственно. Погрешность определения температуры плавления золота и серебра достаточно мала (несколько десятых градуса), для рутения, родия и иридия - несколько градусов для палладия, платины около 10К, а для осмия точных данных нет.
Теплоемкость. Теплоемкость серебра, золота и платины, как правило, определяют на образцах металлов, содержащих менее 0,01% примесей. Остальных драгоценных металлов – на образцах, содержащих несколько сотых процента (до 0,1%) примесей. В первом приближении при средних и высоких температурах влияние примесей на теплоемкость драгоценных металлов подчиняется правилу аддитивности. Погрешность измерения теплоемкости для этих металлов при температурах ниже 300 К обычно составляет 1 – 2%, в диапазоне температур 300 – 1000 К равна 2 – 3%, при более высоких температурах – 5%, а вблизи точки плавления теплоемкость может достигать 10%.
Каждый металл имеет определенную удельную теплоемкость. Зная эту величину, можно легко вычислить количество теплоты, необходимое для нагрева металла от комнатной температуры до температуры плавления. Так как удельная теплоемкость при повышении температуры несколько изменяется, то для расчетов используют ее среднее значение, необходимое для расплавления 1 кг различных металлов. Расчеты показывают, что для расплавления золота требуется относительно небольшое количество тепла, в то время как для меди, несмотря на небольшую разницу в температуре плавления (не больше 20°С), необходимо тройное количество тепла, а для серебра требуется даже больше тепла, чем для золота, хотя оно имеет более низкую температуру плавления. Например, в плавильной установке, после расплавления чистого золота, еще останется большое количество нерасплавленной меди.
Температурное расширение. Каждый металл при нагревании расширяется, а при охлаждении сжимается. Это свойство считается общим для всех металлов, но изменения размеров при изменении температуры у всех металлов различны. Для их определения необходимо знать температурный коэффициент линейного расширения, который характеризует увеличение размера образца длиной 1 м при нагревании на 1 градус. Так, в пластинах, спаянных из золота и серебра, вследствие различия их температурных коэффициентов линейного расширения, возникают напряжения в паяном швепри изменении температуры. Например, при пайке ювелирных изделий из сплавов серебра, скрепленные мягкой стальной проволокой детали, зачастую смещаются, так как температурные коэффициенты линейного расширения этих металлов сильно отличаются по величине.
Известно, что температурный коэффициент линейного расширения стекла очень мал, т.е. примерно такой же, как у платины. Поэтому для того чтобы эмаль держалась на металле, в нее вводят специальные добавки, повышающие этот коэффициент.
Теплопроводность. Из всех металлов наибольшей теплопроводностью обладает серебро, в этом мог убедиться каждый, кто держал в руках серебряную проволоку при ее нагревании. Для характеристики теплопроводности различных материалов пользуются коэффициентом теплопроводности, который имеет размерность Вт/(м·К). Различие в теплопроводности драгоценных металлов необходимо учитывать, например, при пайке деталей ювелирных изделий, изготовленных из разных материалов.
Электросопротивление. Драгоценные металлы І группы периодической системы имеют, по сравнению с металлами платиновой подгруппы, относительно малое удельное электросопротивление. Наибольшей проводимостью из всех известных металлов обладает серебро. Среди драгоценных металлов самое большое удельное электросопротивление имеет платина. Платина характеризуется устойчивой величиной удельного электросопротивления и его температурного коэффициента и применяется для термометров сопротивления. Удельное электросопротивление сильно зависит от содержания и характера примесей, увеличение содержания которых снижает значения проводимости и температурного коэффициента.
Оптические свойства. Отражательная способность у драгоценных металлов различна, поэтому они имеют разный цвет. Так, серебро имеет белый цвет. Золото хорошо отражает дневной свет, однако в желтой области спектра, т.е. при длине световых волн около 5,5∙10–7 м, отражательная способность золота очень незначительна. Этот металл обладает золотисто-желтым цветом и сильным металлическим блеском. В дисперсном состоянии в проходящем свете зеленоватый или голубовато-зеленый, в расплавленном состоянии – зеленый, пары же золота имеют зеленовато-желтый цвет. По сравнению с твердым состоянием расплавленное золото излучает в красном цвете сильнее, чем в голубом. Золото дает со многими металлами химические соединения, обладающие различной окраской. Соединение AuAl2 (78,5%Au + 21,5%Al) имеет фиолетово-пурпурный цвет, AuZn2 – синий цвет, Au2Na - светло-желтый цвет, AuK – оливково-зеленый цвет, Au2K – фиолетовый цвет. С рубидием золото дает аурид Au2Rb – темно-зеленого цвета.
Рутений, палладий и платина имеют серебристо-белый цвет со слабым сероватым оттенком.
Родий имеет белый цвет с голубоватым оттенком. Отражательная способность родия меньше, чем у серебра на 20%, но родиевые покрытия более стойкие в эксплуатации. Родиевые покрытия имеют высокую стойкость против потускнения, хорошую отражательную способность, высокую термическую (до 430°С) и химическую устойчивость. Покрытия, полученные распылением родия в аргоне, или неоне, обладают большей отражательной способностью в области коротких инфракрасных волн, чем полученные распылением в азоте.
Иридий имеет белый цвет с сероватым оттенком, а осмий – оловянно- белый с серо-голубым оттенком.
Сплавы серебра с медью имеют серебристо-белый цвет и сильный блеск. С увеличением количества меди цвет сплавов постепенно переходит от серебристо-белого к желтому (70%Ag), от темного к бледно-красному (50%Ag), от бледно-красного к красному (30%Ag). Цвет сплавов золото – серебро – медь изменяется постепенно от золотисто-желтого (золото) до серебристо-белого (серебро) и до красного (медь); от ярко-красного (золото с медью) до светло- зеленого (золото с серебром). Добавка до 12% палладия (или равноценного по объему количества платины) в золото и золотые сплавы (в том числе и с медью) уничтожает практически полностью специфический для золота и меди цвет, придавая им оттенок, характерный для платиновых металлов. Влияние добавок золота на цвет платиновых металлов незначительно. Так, добавка в палладий до 50% золота, меди, а также цинка, олова и хрома заметно на цвет не влияет. Введение в палладий серебра, никеля, алюминия, родия, рутения и иридия придает сплавам более светлый серебристый оттенок. Наибольшее влияние на цвет оказывают сурьма, марганец, кремний и железо. Сплав, содержащий 50% сурьмы, имеет золотистый, 50% марганца – темно-бурый, 50% кремния - фиолетовый (как у кремния) цвет. Добавка 50% железа придает сплаву темный оттенок. Отражательную способность драгоценных металлов используют при изготовлении бытовых и технических зеркал и в измерительных приборах. Наибольшее отражение видимой части спектра дает серебро, применение которого ограничено недостаточной стойкостью к потускнению. Высокую отражательную способность, сохраняющуюся с изменением длины волны, температуры и атмосферных условий, имеет родий; он применяется для покрытий технических зеркал и рефлекторов. В ряде случаев для покрытий деталей часов, измерительных приборов и технических зеркал используют палладий, имеющий по сравнению с серебром большую устойчивость к потускнению и меньшую стоимость, чем золото и родий. Существуют таблицы с данными о цвете золотых сплавов, применяемых в разных странах.
Химические свойства
Драгоценные металлы в порядке возрастания химической устойчивости в различных средах могут быть расположены в следующем порядке: серебро, палладий и осмий (наименее устойчивы), рутений и родий (весьма устойчивы) и иридий (наиболее устойчив). Введение серебра в палладий, серебра и палладия в другие драгоценные металлы снижает их коррозионную устойчивость. Все драгоценные металлы не окисляются на воздухе при обычной температуре (кроме осмия) и не тускнеют под действием сероводорода и сернистых соединений (кроме серебра). Под действием ртутных соединений, а также паров соляной кислоты происходит коррозионное растрескивание сплавов золота, содержащих медь.
Серебро легко растворяется в концентрированной азотной и горячей серной кислотах. Действие азотной кислоты усиливается с повышением температуры. Серебро стойко в холодных растворах органических кислот, не загрязняет и не изменяет окраски фенола, фруктовых соков, эфирных масел, вина и многих фармацевтических препаратов. Серебро в виде ионов (так называемая серебряная вода) имеет весьма сильное бактерицидное действие. Серебро высоко стойко против коррозии в щелочах и мочевине. Сернистые соединения вызывают коррозию серебра. Потускнение и потеря отражательной способности серебра на воздухе связаны с присутствием сернистых соединений (наряду с влагой и кислородом) и образованием пленки Ag2S. Сухой сероводород не действует на серебро. Увеличение стойкости серебра к потускнению достигается введением цинка, олова, сурьмы и особенно кадмия. Однако эти добавки (обычно составляющие не более 1 – 1,5%) не исключают потемнения данного металла в обычных атмосферных условиях, но значительно повышают его стойкость к потускнению при добавке бериллия (0,5-1,5%). Серебро, содержащее 40% и более палладия, не тускнеет.
Золото растворяется в царской водке и растворе цианистого калия, быстро разрушается в горячих смесях серной и азотной кислот и серной кислоты с окислами тяжелых металлов. Золото частично растворимо при кипячении в азотной кислоте и при нагреве выше 250°С в присутствии кислорода в серной кислоте. Чистое золото стойко в кислороде, сере, сернистом ангидриде и селене. Золото, химически восстановленное из разных растворов, имеет различный вид и цвет. Различные цвета золота могут быть получены восстановлением сернистой кислотой хлорного, хлористого, бромного, бромистого или йодистого золота. Черное золото можно получить растворением золота в амальгаме натрия под водой с последующим подкислением соляной кислотой; коричневое золото растворением серебряно-золотых сплавов. Черное золото растворяется в щелочных растворах быстрее обычного золота. Коричневое золото хорошо растворяется в азотной и соляной кислотах. При растворении в горячей соляной кислоте и последующем охлаждении образуются кристаллы обычного золота.
Рутений устойчив в кислотах и ряде других химически активных средах, в том числе в горячей царской водке, сильно окисляется в щелочах, наиболее агрессивен для этого металла раствор NaClO.
Родий устойчив в кислотах и других химически активных средах, в том числе, в царской водке. При сплавлении со щелочами родий окисляется. Родиевая чернь, получаемая при восстановлении родиевых солей смесью алкоголя и едкого калия или смесью аммиака, муравьиной и уксусной кислот, легко растворяется в присутствии воздуха в концентрированных серной и соляной кислотах и царской водке.
Палладий имеет наибольшую химическую активность по сравнению с другими металлами платиновой группы, растворяется в царской водке и в концентрированной азотной кислоте. В закрытом помещении при обычной температуре палладий не темнеет. В виде сплавов с платиной этот металл служит катализатором ряда химических реакций при получении аммиака, азотной кислоты, лекарственных препаратов и т.д.
Иридий не растворяется в разбавленных и концентрированных кислотах и царской водке, слегка корродирует в царской водке при нагреве до 250–300°С и повышенном давлении. Иридиевые тигли стойки по отношению к расплавленному свинцу и к силикатным расплавам, содержащим окись свинца при 1000–1500°С, в то время как платина растворяется в жидком свинце. Иридий стоек против воздействия фосфатов кальция при 1500 - 1650°С и давлении 10–6–10–7 ат. Платина в этих условиях взаимодействует с фосфором и разрушается.
Иридиевая чернь является катализатором ряда химических реакций, например, образования озона из кислорода, гипохлористой кислоты из кислорода и хлорной воды и т.д.
Осмий растворим в дымящей азотной кислоте и в царской водке. Осмиевая чернь подобно другим платиновым металлам, обладает каталитическим действием: например, вызывает взрыв гремучего газа при 40–50°С, образование аммиака из азота и водорода при 880–1000°С и давлении 185 ат и т.д.
Платина весьма устойчива к действию различных химически активных веществ. При нагревании на воздухе платина не изменяется. Газы, содержащие углерод (метан, окись углерода), не действуют на платину. При нагревании платины в аммиаке она чернеет вследствие отложения на поверхности платиновой черни. Платина в компактном виде (проволока, листы, лента), в виде черни и в коллоидном состоянии представляет собой весьма активный катализатор ряда химических реакций. Содержание в платине никеля не снижает ее каталитического действия, алюминий, кобальт и висмут значительно уменьшают, а медь, цинк, серебро, олово и железо полностью уничтожают это действие.
Механические свойства
Упругие и прочностные свойства. Упругие свойства металлов являются структурно-нечувствительными и связаны с природой сил сцепления атомов, характером связей, кристаллическим строением и т.п. Cеребро, палладий, платина и золото обладают самыми низкими упругими характеристиками, а осмий и иридий – самыми высокими.
Очень важными являются характеристики механических свойств металлов, основными из которых считают твердость - HV(HB), временное сопротивление разрыву – σв, предел текучести – σ0,2 , относительное удлинение
δ, относительное сужение – ψ. Прочностные характеристики драгоценных металлов приведены в табл. 1
Таблица 1. Механические свойства драгоценных металлов технической чистоты в отожженном состоянии
|
Металл |
HV(HB),МПа |
σв, МПа |
σ0,2, МПа |
δ, % |
ψ, % |
|
Ru |
2000 – 3000 |
500 – 600 |
350 – 400 |
3 – 10 |
2 – 3 |
|
Rh |
1000 – 1300 |
400 – 560 |
70 – 100 |
8 – 15 |
20 – 25 |
|
Pd |
380 – 460 |
180 – 200 |
50 – 70 |
25 – 35 |
80 – 85 |
|
Ag |
245 – 250 |
140 – 160 |
20 – 25 |
40 – 50 |
80 – 95 |
|
Os |
3000 – 4000 |
– |
– |
0 |
0 |
|
Ir |
1700 – 2200 |
400 – 500 |
90 – 120 |
6 – 10 |
10 – 15 |
|
Pt |
390 – 420 |
120 – 160 |
60 – 80 |
40 – 50 |
95 – 100 |
|
Au |
220 – 250 |
120 – 130 |
10 – 25 |
45 – 50 |
90 – 95 |
Данные табл. 1 показывают, что достаточно высокой пластичностью (относительное удлинение 30 и более процентов) обладают золото, серебро,
платина и палладий. Если у металла понижена пластичность, то при таких видах обработки металлов давлением, как прокатка, волочение, ковка, штамповка и других, которые обычно используют при получении из них изделий, металл можно подвергать лишь небольшим степеням пластической деформации. При высоких значениях прочности требуются и большие усилия для деформации. Так, например, в ювелирном производстве, при изготовлении колец необходим очень пластичный металл, легко подвергающийся гибке, ковке и вытягиванию отдельных частей кольца. Металл для оправы также должен иметь высокую пластичность, чтобы можно было легко закрепить в ней камень. Однако твердость и износостойкость этого металла не должны быть низкими, иначе камень может выпасть из оправы. Материалы для цепочек должны обладать высокой прочностью и твердостью, чтобы не происходил износ звеньев. Но при этом материал должен быть достаточно пластичным, чтобы звенья цепочки легко гнулись при ее изготовлении.
Основные факторы, влияющие на прочность драгоценных металлов это:
легирование – добавка к чистым металлам легирующих компонентов повышает прочность;
пластическая деформация –холодная пластическая деформация повышает прочность;
величина зерна – мелкозернистая структура придает металлу большую прочность, чем крупнозернистая;
температура – с повышением температуры прочность понижается.
Одним из основных способов получения металлических изделий является пластическая деформация. Для драгоценных металлов и их сплавов, как правило, используют горячую и холодную пластическую деформации. Горячая обработка этих металлов, обычно не имеет самостоятельного значения, предшествует холодной, а в ряде случаев отсутствует. Исключение составляет небольшое количество (по номенклатуре и объему производства) металлов и сплавов.
Применительно к драгоценным металлам и сплавам наиболее распространена холодная деформация. Это связано с тем, что объем производства таких сплавов незначителен, и поэтому вопросы повышения производительности (а с ним связаны необходимость увеличения веса слитка, установка специального оборудования и т.д.) за счет применения горячей деформации не имеют такого значения, как при крупнотоннажном производстве. Холодная пластическая деформация является, как правило, одним из основных этапов производства изделий и полуфабрикатов из драгоценных металлов и сплавов. При холодной деформации (прокатке, прессовании, волочении, объемной и листовой штамповке) обеспечивается высокое качество поверхности, значительная точность геометрических размеров с возможностью получения различных по величине и форме сечений изделий.
Обработка в холодном состоянии требует высоких удельных и общих нагрузок, на которые должны быть рассчитаны инструменты и соответствующие узлы оборудования. Величина этих усилий может быть с достаточной для практики точностью определена, если известны показатели сопротивления деформации (предел текучести, временное сопротивление разрыву) и их зависимость от степени деформации.
Холодную деформацию ведут обычно с промежуточными отжигами. Величину суммарной деформации (от отжига до отжига) выбирают с учетом допустимого упрочнения (повышения сопротивления деформации и снижения пластичности). Кривые зависимости сопротивления упругой и пластической деформации и характеристик пластичности от степени холодной деформации для чистых металлов приведены в справочниках, используя которые, можно выбрать такую степень деформации, чтобы получить необходимый комплекс механических свойств изделия или полуфабриката.
Учитывая сложившиеся в мировой практике, включая и нашу страну, традиционные положения по производству и потреблению драгоценных металлов, можно рекомендовать для практического применения следующую специальную классификацию драгоценных металлов по их химическому составу.
Драгоценные металлы и любые сплавы, содержащие их в качестве компонентов, представляют собой наряду с другими группами металлов и сплавов (например, черных, цветных и т.д.) самостоятельную группу, которую следует именовать в общем виде драгоценные металлы и сплавы.
Делить группы драгоценных металлов и сплавов на основные структурные подразделения (подгруппы) и называть эти подразделения следует по наименованию драгоценных металлов с учетом их количественного (в процентах по массе) содержания в сплавах в качестве компонентов. Иными словами, какой из драгоценных металлов входит в сплавы в превалирующем количестве, относительно других драгоценных металлов, и является основным компонентом этих сплавов. Исключением являются сплавы, содержащие в качестве компонента золото и предназначенные для изготовления изделий бытового назначения, подлежащего компетенции пробирного надзора, в частности сплавы, содержащие 37,5% золота, где оно независимо от содержания других драгоценных металлов считается основным компонентом и определяет наименование сплавов.
Драгоценный металл, содержание которого в данном сплаве максимально, считается и основным компонентом сплавов в целом, т.е. независимо от того, содержится ли он в превалирующем или в меньшем количестве в этих сплавах относительно содержания в них других недрагоценных металлов.
Таким образом, основным компонентом в сплавах, содержащих драгоценные металлы, считается любой драгоценный металл, содержащийся в сплавах в превалирующем количестве относительно других драгоценных металлов и в любом количестве относительно остальных компонентов сплавов.
Легирующими компонентами сплавов драгоценных металлов являются все компоненты сплавов, которые не относятся к драгоценным металлам, а также все компоненты – драгоценные металлы, содержащиеся в сплавах в количествах, меньших, чем основные драгоценные металлы.
В группу драгоценных металлов и сплавов в общем виде входят следующие структурные подразделения (подгруппы): серебро и его сплавы; золото и его сплавы; платина и ее сплавы; палладий и его сплавы; родий и его сплавы; рутений и его сплавы; иридий и его сплавы, и осмий и его сплавы.
К сплавам серебра либо золота, платины, палладия, родия, рутения, иридия, или осмия относятся любые сплавы, в которых каждый из этих металлов соответственно присутствует в качестве компонента в любых количествах, но более содержания других драгоценных металлов.
При этом если сплав содержит одновременно несколько драгоценных металлов в одном и том же количестве, то основным компонентом в таких сплавах следует считать драгоценный металл, определяющий основное назначение данного сплава. Например, в сплаве 50%Ag + 50%Pd, предназначаемом для электрических контактов, следует считать основным компонентом серебро, а сплав именовать серебряным, так как серебро в этом сплаве выполняет основное назначение контакта.
В зависимости от назначения входящих в сплавы компонентов и назначения сплавов в целом сплавы драгоценных металлов могут подразделяться следующим образом:
- основные сплавы, предназначаемые для непосредственного производства полуфабрикатов и изделий из них;
- припойные сплавы или просто припои, предназначаемые для непосредственного производства припойных полуфабрикатов, применяемых в качестве материалов сочленения деталей изделий методом пайки;
- промежуточные сплавы или лигатуры, применяемые в качестве шихтовых материалов для приготовления основных и припойных сплавов с целью сокращения угара легкоплавких составляющих шихт или введения в основной сплав тугоплавких составляющих его компонентов.
В зависимости от сфер потребления и наличия пробирного надзора за содержанием драгоценных металлов в сплавах они подразделяются:
- на металлы аффинированные, предназначаемые для производства полуфабрикатов и изделий, а также специальных целей;
- на металлы и сплавы в полуфабрикатах, предназначаемые для производства полупродуктов, либо изделий промышленного потребления, а также на металлы и сплавы в изделиях такого же характера потребления;
- на металлы и сплавы в полуфабрикатах, предназначаемых для производства основ или деталей изделий, а также в самих изделиях бытового, музейно-выставочного и другого потребления, имеющих обращение у населения и подлежащих в виде изделий обязательному контролю и клеймению органами пробирного надзора.
В свою очередь основные, припойные и промежуточные сплавы серебра, золота, платины и т.д. подразделяются на подгруппы по наименованию этих сплавов, определяемого наименованием входящих в них компонентов. Например, сплавы серебра подразделяются на сплавы серебра с медью, серебра с кадмием, серебра с медью и никелем и т.д.; припои серебряные подразделяются на припои серебра с медью и цинком, серебра с медью и фосфором и т.д.
Классификация драгоценных металлов и всех их сплавов (основных, припойных и промежуточных) завершается в зависимости от их химического состава построением и присвоением металлам и сплавам сокращенных или вообще условных обозначений их качественного (в буквах) и количественного (в буквах или цифрах) химического состава по содержанию основных и легированных (полностью или частично) компонентов.
Для качественной характеристики химического состава по компонентам драгоценных металлов и сплавов в полуфабрикатах и изделиях в их марках применяют следующие обозначения (символы): для компонентов из драгоценных металлов: Ср – серебро, Зл – золото, Пл платина, Пд – палладий, Рд – родий, Ру – рутений, И – иридий, и Ос – осмий, причем все они стандартизованы соответствующими государственными стандартами и согласуются с обозначением других химических элементов;
для других компонентов: М – медь, Н – никель, Ц – цинк, Кд – кадмий, Ол – олово, Мц – марганец, К – кобальт, Кр – кремний, Ф – фосфор, и т.д., которые также узаконены соответствующими стандартами.
Для качественной характеристики химического состава по компонентам драгоценных металлов, полученных аффинированием, в их маркировках применяют частью эти же стандартизированные (для платины и всех платиноидов ), а частью иные, регламентированные только техническими условиями (для серебра и золота) буквенные обозначения, причем с обязательным добавлением ко всем как стандартизированным, так и нестандартизированным символам дополнительного символа А, обозначающего, что данный металл аффинированный, например, СА – серебро аффинированное, ЗА – золото аффинированное, но ПлА – платина аффинированная, ПдА – палладий аффинированный и т.д. Это может вносить некоторую путаницу в написании марок, так, например, С обозначает и свинец,
Для количественной характеристики химического состава по компонентам аффинированных драгоценных металлов в их марках применяют условные буквенные и численные символы, характеризующие степень чистоты этих металлов. Для серебра и золота: О – особая, 1 – высокая, 2 и 3 – повышенной чистоты и т.д. Для платины и платиноидов: Э – экстра или особая или высокая, 1 и 2 – повышенная чистота и т.д.
При построении марок аффинированных драгоценных металлов по данной классификации и терминологии количественные символы проставляют за качественными через дефис, например, СА-О, СА-1 и т.д., ЗА-1, ЗА-2, ПлА-Э, ПлА-1 и т.д.
Химический состав всех металлов и сплавов выражается в процентах по массе. В государственных стандартах и технических условиях, устанавливающих марки металлов и сплавов и регламентирующих их химический состав, он дается, развернуто по всем компонентам и примесям в технической характеристике металлов и сплавов и сокращенно только по компонентам основным и легирующим или их части в марках этих металлов и сплавов. Однако, согласно традициям, сложившимся, как в нашей стране, так и за рубежом, а также в соответствии с положениями о пробирном надзоре, установленном правительствами многих стран, в этом правиле делают исключения для золота, серебра, платины, палладия и сплавов этих металлов между собой и с другими металлами. Исключение составляют полуфабрикаты и получаемые из них изделия: ювелирно-бытового назначения (кольца, серьги, броши, колье, цепи, браслеты, часы и подобные им украшения; чайная и столовая посуда и приборы; бокалы, зажигалки, шкатулки и другие предметы домашнего обихода), памятные и нагрудные (кубки, барельефы, значки, номограммы, медали, ордена и т.п.) и прочие предметы, поступающие в обращение к населению, либо для музейно-выставочного назначения. Сущность этого отступления состоит в том, что за единицу размерности содержания драгоценных металлов в марках этих металлов и сплавов принимаются не проценты по массе, а пробы. Проба представляет собой число частей характеризуемого ею металла в единице массы этого металла или содержащего его сплава, соответствующей данной системе весовых измерений, поэтому по своему числовому выражению пробы или системы проб не одинаковы для различных систем весовых измерений. Так как в разные периоды времени в различных странах применялись и до сих пор применяются различные системы весовых измерений, то соответственно им существовали и в ряде стран продолжают еще существовать и сейчас разные системы проб драгоценных металлов и их сплавов.
Построение марок сплавов в полуфабрикатах и изделиях с количественной характеристикой компонентов в пробах аналогично построению марок сплавов, где компоненты характеризуются в процентах по массе, например Ср999, Зл999,9 и т.д. В марках сплавов, где характеристика их количественного состава дается в пробах, она приводится только для драгоценных металлов, причем, начиная с основного, а не со второго. При этом первый количественный символ проставляется вплотную без дефиса к последнему качественному символу, а затем уже проставляется через дефис количество всех других компонентов, например СрМ875, ЗлСр750-250, ЗлСрМ583-80 и т.д. Что касается компонентов, содержащихся в сплавах, но не относящихся к драгоценным металлам, то в марках этих сплавов их количественная характеристика не приводится. Указанное можно объяснить тем, что в эти сплавы входит обычно один такой компонент, в частности медь или он вообще отсутствует.
Ценные свойства цветных металлов обусловили их широкое применение в различных отраслях современного производства. Медь, алюминий, цинк, магний, титан и другие металлы и их сплавы являются незаменимыми материалами для приборостроительной и электротехнической промышленности, самолетостроения и радиоэлектроники, ядерной и космической отраслей техники. Цветные металлы обладают рядом ценных свойств: высокой теплопроводностью, очень малой плотностью (алюминий и магний), очень низкой температурой плавления (олово, свинец), высокой коррозионной стойкостью (титан, алюминий). В различных отраслях промышленности широко применяются сплавы алюминия с другими легирующими элементами.
Сплавы на магниевой основе отличаются малой плотностью, высокой удельной прочностью, хорошо обрабатываются резанием. Они нашли широкое применение в машиностроении и в частности в авиастроении.
Техническая медь, содержащая не более 0,1 % примесей, применяется для различных видов проводников тока.
Медные сплавы по химическому составу классифицируются на латуни и бронзы. В свою очередь латуни по химическому составу подразделяются на простые, легированные только цинком, и специальные, которые, помимо цинка, содержат в качестве легирующих элементов свинец, олово, никель, марганец.
Бронзы также подразделяются на оловянные и безоловянные. Безоловянные бронзы имеют высокую прочность, хорошие антикоррозионные и антифрикционные свойства.
В металлургии широко используется магний, с помощью которого осуществляют раскисление и обессеривание некоторых металлов и сплавов, модифицируют серый чугун с целью получения графита шаровидной формы, производят трудно восстанавливаемые металлы (например, титан), смеси порошка магния с окислителями служат для изготовления осветительных и зажигательных ракет в реактивной технике и пиротехнике. Свойства магния значительно улучшаются за счет легирования. Алюминий и цинк с массовой долей до 7 % повышают его механические свойства, марганец улучшает его сопротивление коррозии и свариваемость, цирконий, введенный в сплав вместе с цинком, измельчает зерно (в структуре сплава), повышает механические свойства и сопротивление коррозии.
Из магниевых сплавов изготавливают фасонные отливки, а также полуфабрикаты – листы, плиты, прутки, профили, трубы, проволоки. Промышленный магний получают электролитическим способом из магнезита, доломита, карналлита, морской воды и отходов различного производства по схеме получение чистых безводных солей магния, электролиз этих солей в расплавленном состоянии и рафинирование магния В природе мощные скопления образуют карбонаты магния – магнезит и доломит, а также карналлиты.
В пищевой промышленности широко применяется упаковочная фольга из алюминия и его сплавов – для обертки кондитерских и молочных изделий, а также в больших количествах используется алюминиевая посуда (пищеварочные котлы, поддоны, ванны и т. д.).
Медные сплавы
Медь относится к числу металлов, известных с глубокой древности. Раннему знакомству человека с медью способствовало то, что она встречается в природе в свободном состоянии в виде самородков, которые иногда достигают значительных размеров. В настоящее время медь широко используется в электромашиностроении, при строительстве линий электропередач, для изготовления оборудования телеграфной и телефонной связи, радио—и телевизионной аппаратуры. Из меди изготовляют провода, кабели, шины и другие токопроводящие изделия. Медь обладает высокой электропроводностью и теплопроводностью, прочностью вязкостью и коррозионной стойкостью. Физические свойства ее обусловлены структурой. Она имеет кубическую гра—нецентрированную пространственную решетку. Ее температура плавления – +1083 °C, кипения – +2360 °C. Средний предел прочности зависит от вида обработки и составляет от 220 до 420 МПа (22–45 кгс/мм 2), относительное удлинение – 4—60 %, твердость – 35—130 НВ, плотность – 8,94 г/см 3. Обладая замечательными свойствами, медь в то же время как конструкционный материал не удовлетворяет требованиям машиностроения, поэтому ее легируют, т. е. вводят в сплавы такие металлы, как цинк, олово, алюминий, никель и другие, за счет чего улучшаются ее механические и технологические свойства. В чистом виде медь применяется ограниченно, более широко – ее сплавы. По химическому составу медные сплавы подразделяют на латуни, бронзы и медноникелевые, по технологическому назначению – на деформируемые, используемые для производства полуфабрикатов (проволоки, листа, полос, профиля), и литейные, применяемые для литья деталей.
Латуни – сплавы меди с цинком и другими компонентами. Латуни, содержащие, кроме цинка, другие легирующие элементы, называются сложными, или специальными, и именуются по вводимым, кроме цинка, легирующим компонентам. Например: томпак Л90 – это латунь, содержащая 90 % меди, остальное – цинк; латунь алюминиевая ЛА77–2 – 77 % меди, 2 % алюминия, остальное – цинк и т. д. По сравнению с медью латуни обладают большой прочностью, коррозионной стойкостью и упругостью. Они обрабатываются литьем, давлением и резанием. Из них изготовляют полуфабрикаты (листы, ленты, полосы, трубы конденсаторов и теплообменников, проволоку, штамповки, запорную арматуру – краны, вентили, медали и значки, художественные изделия, музыкальные инструменты, сильфоны, подшипники).
Бронзы – сплавы на основе меди, в которых в качестве добавок используются олово, алюминий, бериллий, кремний, свинец, хром и другие элементы. Бронзы подразделяются на безоловянные (БрА9Мц2Л и др.), оловянные (БрО3ц12С5 и др.), алюминиевые (БрА5, БрА7 и др.), кремниевые (БрКН1–3, БрКМц3–1), марганцевые (БрМц5), бериллиевые бронзы (БрБ2, БрБНТ1,7 и др.). Бронзы используются для производства запорной арматуры (краны, вентили), различных деталей, работающих в воде, масле, паре, слабоагрессивных средах, морской воде.
Алюминиевые сплавы
Название «алюминий» происходит от латинского слова alumen – так за 500 лет до н. э. называли алюминиевые квасцы, которые использовались для протравливания при крашении тканей и дубления кож.
По распространенности в природе алюминий занимает третье место после кислорода и кремния и первое место среди металлов. По использованию в технике он занимает второе место после железа. В свободном виде алюминий не встречается, его получают из минералов – бокситов, нефелинов и алунитов, при этом сначала производят глинозем, а затем из глинозема путем электролиза получают алюминий. Механические свойства алюминия невысоки: сопротивление на разрыв – 50–90 МПа (5–9 кгс/мм 2), относительное удлинение – 25–45 %, твердость – 13–28 НВ.
Алюминий хорошо сваривается, однако трудно обрабатывается резанием, имеет большую линейную усадку – 1,8 % В чистом виде алюминий применяется редко, в основном широко используются его сплавы с медью, магнием, кремнием, железом и т. д. Алюминий и его сплавы необходимы для авиа—и машиностроения, линий электропередач, подвижного состава метро и железных дорог.
Алюминиевые сплавы подразделяются на литейные и деформируемые. Литейные сплавы алюминия выпускаются в чушках – рафинированные и нерафинированные.
Сплавы, в обозначении марок которых имеется буква «П», предназначены для изготовления пищевой посуды. Механические свойства сплавов зависят от их химического состава и способов получения. Химический состав основных компонентов, входящих в сплав, можно определить по марке. Например, сплав АК12 содержит 12 % кремния, остальное – алюминий; АК7М2П – 7 % кремния, 2 % меди, остальное – алюминий. Наиболее широко применяется в различных отраслях промышленности сплав алюминия с кремнием – силумин, который изготовляется четырех марок – СИЛ–00, СИЛ–0, СИЛ–1 и СИЛ–2. Кроме алюминия (основа) и кремния (10–13 %), в этот сплав входят: железо – 0,2–0,7 %, марганец – 0,05—0,5 %, кальций – 0,7–0,2 %, титан – 0,05—0,2 %, медь – 0,03 % и цинк – 0,08 %. Из силуминов изготовляют различные детали для автомобилей, тракторов, пассажирских вагонов. Алюминиевые деформируемые сплавы в чушках, предназначенные для обработки давлением и для подшик—товки при получении других алюминиевых сплавов, нормируются определенными стандартами. Сплавы для обработки давлением состоят из алюминия (основа), легирующих элементов (медь – 5 %, магний – 0,1–2,8 %, марганец – 0,1–0,7 %, кремний – 0,8–2,2 %, цинк – 2–6,5 % и небольшого количества других примесей). Марки этих сплавов: ВД1, АВД1, АВД1–1, АКМ, из алюминиевых сплавов изготавливают полуфабрикаты – листы, ленты, полосы, плиты, слитки, слябы.
Кроме того, цветная металлургия производит алюминиевые антифрикционные сплавы, применяемые для изготовления монометаллических и биметаллических подшипников методом литья. В зависимости от химического состава стандартом предусмотрены следующие марки этих сплавов: АО3–7, АО9–2, АО6–1, АО9–1, АО20–1, АМСТ. Стандартом также определены условия работы изделий, изготовленных из этих сплавов: нагрузка от 19,5 до 39,2 МН/м2 (200–400 кгс/см 2), температура от 100 до 120 °C, твердость – от 200 до 320 НВ.
Титановые сплавы
Титан – металл серебристо—белого цвета. Это один из наиболее распространенных в природе элементов. Среди других элементов по распространенности в земной коре (0,61 %) он занимает десятое место. Титан легок (плотность его 4,5 г/см 3), тугоплавок (температура плавления 1665 °C), весьма прочен и пластичен. На поверхности его образуется стойкая окисная пленка, за счет которой он хорошо сопротивляется коррозии в пресной и морской воде, а также в некоторых кислотах. При температурах до 882 °C он имеет гексагональную плотно упакованную решетку, при более высоких температурах – объемно—центрированный куб. Механические свойства листового титана зависят от химического состава и способа термической обработки. Предел прочности его – 300—1200 МПа (30—120 КГС/мм 2), относительное удлинение – 4—10 %. Вредными примесями титана являются азот, углерод, кислород и водород. Они снижают его пластичность и свариваемость, повышают твердость и прочность, ухудшают сопротивление коррозии.
При температуре свыше 500 °C титан и его сплавы легко окисляются, поглощая водород, который вызывает охрупчи—вание (водородная хрупкость). При нагревании выше 800 °C титан энергично поглощает кислород, азот и водород, эта его способность используется в металлургии для раскисления стали. Он служит легирующим элементом для других цветных металлов и для стали.
Благодаря своим замечательным свойствам титан и его сплавы нашли широкое применение в авиа-, ракето—и судостроении. Из титана и его сплавов изготовляют полуфабрикаты: листы, трубы, прутки и проволоку. Основными промышленными материалами для получения титана являются ильменит, рутил, перовскит и сфен (титанит). Технология получения титана сложна, трудоемка и длительна: сначала вырабатывают титановую губку, а затем путем переплавки в вакуумных печах из нее производят ковкий титан.
Губчатый титан, получаемый магнийтермическим способом, служит исходным материалом для производства титановых сплавов и других целей. В зависимости от химического состава и механических свойств стандартом установлены следующие марки губчатого титана: ТГ–90, ТГ–100, ТГ–110, ТГ–120, ТГ–130. В обозначении марок буквы «ТГ» означают – титан губчатый, «Тв» – твердый, цифры означают твердость по Бринеллю. В губчатый титан входят примеси: железо – до 0,2 %, кремний – до 0,04 %, никель – до 0,05 %, углерод – до 0,05 %, хлор – до 0,12 %, азот – до 0,04 %, кислород – до 0,1 %. Для изготовления различных полуфабрикатов (листы, трубы, прутки, проволока) предназначены титан и титановые сплавы, обрабатываемые давлением. В зависимости от химического состава стандарт предусматривает следующие их марки: ВТ1–00, ВТ1–0, ОТ4–0, ОТ4–1, ОТ4, ВТ5, ВТ5–1, ВТ6, ВТ20, ВТ22, ПТ–7М, ПТ–7В, ПТ–1 м. Основные компоненты: алюминий – 0,2–0,7 %, марганец – 0,2–2 %, молибден – 0,5–5,5 %, ванадий – 0,8–5,5 %, цирконий – 0,8–3 %, хром – 0,5–2,3 %, олово – 2–3 %, кремний – 0,15—0,40 %, железо – 0,2–1,5 %. Железо, кремний и цирконий в зависимости от марки сплава могут быть основными компонентами или примесями.
Цинковые сплавы
Сплав цинка с медью – латунь – был известен еще древним грекам и египтянам. Но выплавка цинка в промышленных масштабах началась лишь в XVII в.
Цинк – металл светло—серо—голубоватого цвета, хрупкий при комнатной температуре и при 200 °C, при нагревании до 100–150 °C становится пластичным.
В соответствии со стандартом цинк изготовляется и поставляется в виде чушек и блоков массой до 25 кг. Стандарт устанавливает также марки цинка и области их применения: ЦВ00 (содержание цинка – 99,997 %) – для научных целей, получения химических реактивов, изготовления изделий для электротехнической промышленности; ЦВО (цинка – 99,995 %) – для полиграфической и автомобильной промышленности; ЦВ1, ЦВ (цинка – 99,99 %) – для производства отливок под давлением, предназначенных для изготовления деталей особо ответственного назначения, для получения окиси цинка, цинкового порошка и чистых реактивов; ЦОА (цинка 99,98 %), ЦО (цинка 99,975 %) – для изготовления цинковых листов, цинковых сплавов, обрабатываемых давлением, белил, лигатуры, для горячего и гальванического цинкования; Ц1С, Ц1, Ц2С, Ц2, Ц3С, Ц3 – для различных целей.
В промышленности широко применяются цинковые сплавы: латуни, цинковые бронзы, сплавы для покрытия различных стальных изделий, изготовления гальванических элементов, типографские и др. Цинковые сплавы в чушках для литья нормируются стандартом. Эти сплавы используются в автомобиле—и приборостроении, а также в других отраслях промышленности. Стандартом установлены марки сплавов, их химический состав, определены изготовляемые из них изделия:
1) ЦАМ4–10 – особо ответственные детали;
2) ЦАМ4–1 – ответственные детали;
3) ЦАМ4–1В – неответственные детали;
4) ЦА4О – ответственные детали с устойчивыми размерами;
5) ЦА4 – неответственные детали с устойчивым размерами.
Цинковые антифрикционные сплавы, предназначенные для производства монометаллических и биметаллических изделий, а также полуфабрикатов, методами литья и обработки давлением нормируются стандартом. Механические свойства сплавов зависят от их химического состава: предел прочности ?В = 250–350 МПа (25–35 КГС/мм 2), относительное удлинение ? = 0,4—10 %, твердость – 85—100 НВ. Стандарт устанавливает марки этих сплавов, области их применения и условия работы: ЦАМ9–1,5Л – отливка монометаллических вкладышей, втулок и ползунов; допустимые: нагрузка – 10 МПа (100 кгс/см 2), скорость скольжения – 8 м/с, температура 80 °C; если биметаллические детали получают методом литья при наличии металлического каркаса, то нагрузка, скорость скольжения и температура могут быть увеличены до 20 МПа (200 КГС/см 2), 10 м/с и 100 °C соответственно: ЦАМ9–1,5 – получение биметаллической ленты (сплав цинка со сталью и дюралюминием) методом прокатки, лента предназначена для изготовления вкладышей путем штамповки; допустимые: нагрузка – до 25 МПА (250 кгс/см 2), скорость скольжения – до 15 м/с, температура 100 °C; АМ10–5Л – отливка подшипников и втулок, допустимые: нагрузка – 10 МПа (100 КГС/см 2), скорость скольжения – 8 м/с, температура 80 °C.
Пластическими массами (пластмассами) называют материалы на основе природных или синтетических высокомолекулярных соединений, из которых получают изделия методами пластической деформации путем нагревания и давления. Они сохраняют свою форму после охлаждения и отверждения.
В состав пластмасс входят:
• основа — полимерное связующее (смолы);
• наполнители;
• катализаторы;
• пластификаторы;
• стабилизаторы;
• красители и другие добавки.
На рис. 3.2 представлена классификация пластмасс.
Термопласты производят на основе термореактивных смол — полиэфиров: фенолформальдегидных, аминоальгидных, эпоксидных, полиамидных, кремнийорганических, ненасыщенных. Пластмассы на основе этих смол отличаются повышенной прочностью, не склонны к ползучести и способны работать при повышенных температурах. Термопласты обычно изготовляют без наполнителя. Из большой группы таких пластмасс основными являются: полиэтилен, поливинилхлорид, полиамиды (нейлон, капрон), полистирол, органическое стекло, фторопласт-4. Из термопластов изготовляют литьевые, пленочные и листовые изделия, которые обладают хорошими электроизоляционными свойства-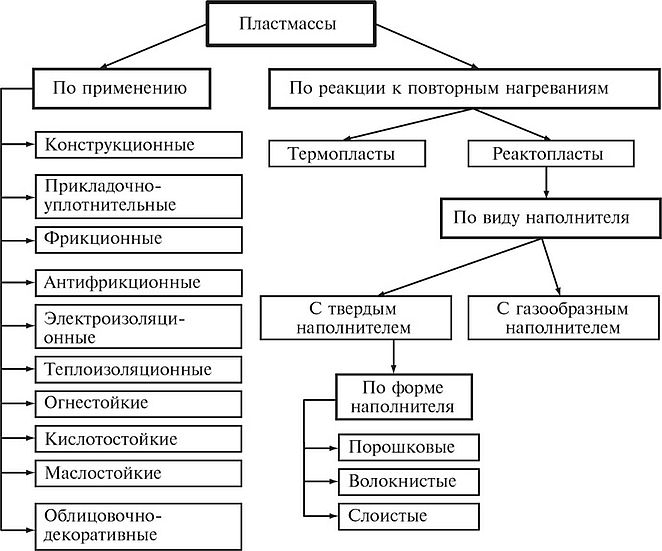
Рисунок 1. Классификация пластмасс
ми, химически стойки в агрессивных средах и к атмосферным воздействиям, отличаются высокой стойкостью к истиранию, вибрации. Однако термопласты обладают хладотекучестью, поэтому изделия из них не могут долго работать под напряжением вследствие понижения их прочности.
Реактопласты характеризуются отсутствием хладотекучести, большой теплостойкостью и нерастворимостью в обычных растворителях. Основу реактопластов составляют смолы: фенолформальдегидная, эпоксидная, кремнийорганическая и др.
В зависимости от формы частиц наполнителя реактопласты можно разделить на следующие группы: порошковые, волокнистые и слоистые. В качестве порошковых наполнителей применяют древесную муку, молотый кварц, слюду, асбест и др. Порошковые пластмассы применяют для несиловых конструкционных и электроизоляционных деталей.
К пластмассам с волокнистыми наполнителями относятся волокиты, асбоволокниты, стекловолокниты. Волокиты применяют для изготовления деталей общего технического назначения (рукояток, фланцев, шкивов и др.), асбоволокниты используют в качестве материала тормозных устройств, стекловолокниты — для изготовления силовых электротехнических деталей, деталей машиностроения.
Слоистые пластмассы являются силовыми конструкционными и поделочными материалами. К ним относятся гетинакс, текстолит, древеснослоистые пластики (ДСП), асботекстолит, стеклопластики. Гетинакс используют в качестве прокладок или плат для приборов электрооборудования, внутренней облицовки пассажирских кабин самолетов, железнодорожных вагонов, кают судов, в строительстве. Текстолит как конструкционный материал применяют для зубчатых колес газораспределительного вала.
Древеснослоистые пластики имеют высокие физико-механические свойства, низкий коэффициент трения. Они с успехом заменяют текстолит и цветные сплавы. ДСП применяют при изготовлении внутренних панелей автобусов, сидений автомобилей.
Асботекстолит является одновременно конструкционным, фрикционным и термоизоляционным материалом. Из него изготавливают фрикционные диски, тормозные колодки, лопатки ротационных бензонасосов.
Промышленность выпускает большое число марок стеклопластиков для различного применения с разными наполнителями (стеклоткань или стеклянный шпон) и связующими. Они отличаются большим разнообразием свойств, однако все обладают высокой прочностью, низкой плотностью, высокими электро-, тепло- и звукоизоляционными свойствами, химической стойкостью. Их применяют в качестве несущих деталей летательных аппаратов, для изготовления автоцистерн, железнодорожных вагонов, корпусов лодок и др.
К газонаполненным пластмассам относятся пенопласты, поропласты и сотопласты. Они отличаются чрезвычайно низкой плотностью и высокими теплозвукоизоляционными свойствами.
Газонаполненные пластмассы используют как амортизационный материал в сидениях автомобилей, а также в качестве теплоизоляционных материалов, например в цельнометаллических рефрижераторных полуприцепах, для звукоизоляции кабин тракторов, экскаваторов и других машин.
Резиновые материалы — особый вид пластмасс (реакто- пласты с редкосетчатой структурой), когда связывающий полимер, каучук натуральный (НК) или синтетический (СК), находится в высокоэластичном состоянии. Свойства резины: высокая эластичность, хорошие амортизационные свойства, сильно выражена зависимость механических свойств от температуры (термическое старение резины: с повышением температуры прочность падает).
При динамическом нагружении свойства резин определяют упруго-гистерезисными (остаточная деформация) и усталостно-прочностными характеристиками. Морозостойкость резины определяется температурой хрупкости ?х и коэффициентом морозостойкости Км.
Резиновые материалы — сложные вещества, в состав которых кроме каучука, входят ускорители вулканизации, наполнители, пластификаторы, противостарители и красители.
Наполнители — вулканизирующие вещества до 30% об. (сера, оксиды цинка, перекисные и нитросоединения) участвуют в создании макромолекул резины. Активные наполнители — сажа, оксид кремния повышают прочность и твердость резины, ее износостойкость. Инертные наполнители — тальк, мел и др. вводят с целью удешевления резины. Пластификаторы — вазелин, парафин, стеариновая кислота, различные масла (до 30% об.) увеличивают эластичность и морозостойкость. Противостарители химического (альдоль, неозон) и физического (парафин, воск) действия, которые, взаимодействуя с кислородом или затрудняя его диффузию из воздуха, препятствуют присоединению кислорода к месту двойной связи в каучуке и ее разрыву, который приводит к потере эластичности и охрупчиванию резины. Красители исполняют декоративные функции и задерживают световое старение.
Резиновые материалы делятся на резины общего и специального назначения.
Резины общего назначения выпускаются на основе каучука с неполярными связями (бутадиеновый каучук — СКВ, бутадиеностирольный — СКС-10, СКС-30, дивинильный) для работы в водной и воздушной средах, в слабых растворах кислот и щелочей, в спирте, ацетоне, жирных кислотах. Интервал рабочих температур: -50...+130 °С. Эти резины, особенно мягкие, не стойки к светоозонному и тепловому старению. Они набухают при контакте с жирными и ароматическими растворителями (бензин, керосин, масло и т.д.). Предназначены для шин авиа- и автоколес, протекторов, покрышек, прокладок, обычных шлангов, амортизаторов и т.д. Марки резин общего назначения — 15РИ 10, МРИ 32456.
Резины специального назначения — обладают негорючестью, морозостойкостью, теплостойкостью, озоностойкос- тью, электропроводностью, а также стойкостью к горючесмазочным материалам. Резины, стойкие к действию озона и света, изготовлены на основе хлоропренового каучука (наирит) и бутилкаучука (БК) с изобутиленом. Марки резины специального назначения — 3826, НО-68-1, В-14-1, ИРП 1287, ИРП 1338.
Силикатными материалами и изделиями называются необожженные материалы и изделия на основе минеральных вяжущих - асбестоцементные, гипсовые и гипсобетонные, силикатные (на основе извести) и магнезиальные с заполнителями (кварцевым песком, шлаком, золой, пемзой, опилками и т. д.). Области применения их чрезвычайно обширны - от несущих и ограждающих конструкций до отделки зданий и сооружений.
Силикатные изделия получают в результате формования и последующей автоклавной обработки смеси извести или других вяжущих веществ на ее основе, тонкодисперсных кремнеземистых добавок, песка и воды.
Силикатный кирпич - искусственный каменный материал, изготовляемый из смеси кварцевого песка и извести путем прессования под большим давлением и последующего твердения в автоклаве. Исходными материалами являются воздушная известь - 6-8% в расчете на СаО, кварцевый песок - 92-94% и вода - 7-8% по массе сухой смеси.
Существуют две схемы производства силикатного кирпича: силосная и барабанная. По силосной схеме известь, совместно с песком, гасят в силосах в течение 4-8 ч. По барабанной схеме известь, совместно с песком, гасят во вращающихся барабанах с подводом пара под избыточным давлением до 0,5 МПа благодаря чему процесс гашения длится 30-40 мин.
Погашенная смесь извести и песка увлажняется, перемешивается и прессуется под давлением 15-20 МПа, в результате получается сырец, который укладывают на вагонетки и направляют в автоклавы на 10-14 ч для запаривания под давлением насыщенного пара 0,8 МПа (изб.) при температуре около 175оС. Прочность силикатного кирпича растет в течение некоторого времени и после выгрузки из автоклава (на воздухе).
Силикатный кирпич выпускают двух видов: одинарный (размером 250х120х65 мм) и модульный (размером 250х120х88 мм). Модульный кирпич изготавливают с технологическими пустотами, замкнутыми с одной стороны. Цвет кирпича светло-серый, но он может быть и цветным за счет введения в состав смеси щелочестойких минеральных пигментов.
Благодаря прессованию под большим давлением и отсутствию усадочных явлений размеры силикатного кирпича выдержаны более точно, чем у глиняного. Плотность его несколько выше, чем у керамического кирпича - 1800-1900 кг/м3, теплопроводность - 0,82 - 0,87 Вт/(м оС). В зависимости от предела прочности при сжатии и изгибе силикатный кирпич изготавливают шести марок: 75, 100, 125, 150, 200 и 250. Морозостойкость силикатного кирпича не ниже Мрз 15, водопоглощение 8-16% по массе.
Области применения силикатного кирпича такие же, как и керамического кирпича. Однако он не рекомендуется для кладки фундаментов и стен в условиях высокой влажности, так как воздействие грунтовых и сточных вод вызывает его разрушение. Нельзя использовать силикатный кирпич в конструкциях, подверженных действию высоких температур (в печах, дымовых трубах и т. п.).
Силикатными бетонами называют большую группу бетонов автоклавного твердения, получаемых на основе известково-песчаного, известково-зольного или других известково-кремнеземистых вяжущих. Кроме того, в качестве вяжущего могут использовать молотые доменные шлаки.
Плотный мелкозернистый силикатный бетон, в отличие от тяжелого бетона, в своем составе не содержит крупного заполнителя (гравия или щебня). Структура силикатного бетона более однородна, а стоимость значительно ниже.
Прочность его при сжатии колеблется в довольно широких пределах (15-60 МПа) и зависит от состава смеси, режима автоклавной обработки и других факторов. Водостойкость силикатного бетона удовлетворительная. При полном водонасыщении снижение их прочности не превышает 25%. Морозостойкость - 25-50 циклов, а при добавке портландцемента она повышается до 100 циклов.
Из плотного силикатного бетона выполняют крупные стеновые блоки наружных стен с щелевыми пустотами и внутренних несущих стен, панели и плиты перекрытий, колонны, балки и прогоны, лестничные площадки и марши, цокольные блоки и другие армированные изделия.
В легких силикатных бетонах в качестве заполнителей используют керамзит, гранулированный шлак, шлаковую пемзу и другие пористые материалы в виде гравия и щебня. Из легких силикатных бетонов на пористых заполнителях изготовляют блоки и панели наружных стен жилых зданий.
Ячеистые силикатные бетоны, в зависимости от способа образования пористой структуры, разделяют на пено- и газосиликаты. Их получают при автоклавной обработке известково-песчаной пластичной смеси, в состав которой вводят устойчивую пену (пеносиликат) или алюминиевую пудру и другие газообразователи (газосиликат).
По назначению легкие и ячеистые силикатные бетоны делят на : теплоизоляционные, конструкционно-теплоизоляционные и конструкционные.
Изделия из силикатобетона не рекомендуются для конструкций, подверженных значительному увлажнению (фундаментов, цоколей, подоконников, карнизов и др.).
. Композиционные или композитные материалы – материалы будущего.
После того как современная физика металлов подробно разъяснила нам причины их пластичности, прочности и ее увеличения, началась интенсивная систематическая разработка новых материалов. Это приведет, вероятно, уже в вообразимом будущем к созданию материалов с прочностью, во много разпревышающей ее значения у обычных сегодня сплавов. При этом большое внимание будет уделяться уже известным механизмам закалки стали и старения алюминиевых сплавов, комбинациям этих известных механизмов с процессами формирования и многочисленными возможностями создания комбинированных материалов. Два перспективных пути открывают комбинированные материалы, усиленные либо волокнами, либо диспергированными твердыми частицами. Упервых в неорганическую металлическую или органическую полимерную матрицу введены тончайшие высокопрочные волокна из стекла, углерода, бора, бериллия, стали или нитевидные монокристаллы. В результате такого комбинирования максимальная прочность сочетается с высоким модулем упругости и небольшой плотностью. Именно такими материалами будущего являются композиционные материалы.
Композиционный материал – конструкционный (металлический или неметаллический) материал, в котором имеются усиливающие его элементы ввиде нитей, волокон или хлопьев более прочного материала. Примеры композиционных материалов: пластик, армированный борными, углеродными, стеклянными волокнами, жгутами или тканями на их основе; алюминий, армированный нитями стали, бериллия. Комбинируя объемное содержание компонентов, можно получать композиционные материалы с требуемымизначениями прочности, жаропрочности, модуля упругости, абразивной стойкости, а также создавать композиции с необходимыми магнитными, диэлектрическими, радиопоглощающими и другими специальными свойствами.
Композиционные материалы с металлической матрицей.
Композитные материалы или композиционные материалы состоят из металлической матрицы (чаще Al, Mg, Ni и их сплавы), упрочненной высокопрочными волокнами (волокнистые материалы) или тонкодисперсными тугоплавкими частицами, не растворяющимися в основном металле (дисперсно-упрочненные материалы). Металлическая матрица связывает волокна (дисперсные частицы) в единое целое. Волокно (дисперсные частицы) плюс связка (матрица), составляющие ту или иную композицию, получили название композиционные материалы.
Композиционные материалы с неметаллической матрицей.
Композиционные материалы с неметаллической матрицей нашли широкое применение. В качестве неметаллических матриц используют полимерные, углеродные и керамические материалы. Из полимерных матриц наибольшее распространение получили эпоксидная, фенолоформальдегидная и полиамидная.
Угольные матрицы коксованные или пироуглеродные получают из синтетических полимеров, подвергнутых пиролизу. Матрица связывает композицию, придавая ейформу. Упрочнителями служат волокна: стеклянные, углеродные, борные, органические, на основе нитевидных кристаллов (оксидов, карбидов, боридов,нитридов и других), а также металлические (проволоки), обладающие высокой прочностью и жесткостью.
Свойства композиционных материалов зависят от состава компонентов,их сочетания, количественного соотношения и прочности связи между ними.
Армирующие материалы могут быть в виде волокон, жгутов, нитей, лент, многослойных тканей.
Содержание упрочнителя в ориентированных материалах составляет 60-80 об. %, в неориентированных (с дискретными волокнами и нитевидными кристаллами) – 20-30 об. %. Чем выше прочность и модуль упругости волокон,тем выше прочность и жесткость композиционного материала. Свойства матрицы определяют прочность композиции при сдвиги и сжатии и сопротивление усталостному разрушению.
По виду упрочнителя композитные материалы классифицируют настекловолокниты, карбоволокниты с углеродными волокнами, бороволокниты иоргановолокниты.
В слоистых материалах волокна, нити, ленты, пропитанные связующим, укладываются параллельно друг другу в плоскости укладки. Плоские слоисобираются в пластины.
